Tel que mentionné dans l’article précédent, l’autophagie joue un rôle majeur pour notre santé et elle constitue une forme d’adaptation cellulaire pour divers types de stress. Ici, le stress est défini comme un facteur qui change les conditions homéostatiques (l’équilibre essentiel à la vie) où le corps doit s’adapter pour retrouver cet équilibre (comme la résistance à la température ou encore à l’oxydation; ce qui peut endommager le fonctionnement cellulaire). Il devient évident maintenant, en considérant l’importance de l’autophagie, que les scientifiques désirent développer des moyens de moduler ces mécanismes, afin de pouvoir les utiliser pour des applications santé. Dans cet article, je vais parler spécifiquement de l’effet d’un stress précis; le stress cellulaire provoqué par le jeûne.
Je commencerai par mentionner les différents facteurs qui stimulent l’autophagie afin de clarifier pourquoi le jeûne devrait être considéré comme un modulateur puissant. Il y a de multiples stimulus qui déclenchent le processus d’autophagie dont :
- Le stress nutritionnel/énergétique
- Les stimuli reliés à des pathogènes particuliers
- Le stress oxydatif
- Le stress du réticulum endoplasmique
- L’hypoxie (manque d’oxygène dans les tissus)
- L’accumulation de protéines mal repliées
- L’ADN et/ou les dommages mitochondriaux
Comme vous pouvez le voir ici, le stress nutritionnel/énergétique est un stimulus qui déclenche le processus d’autophagie. Est-ce que cette stimulation a des conséquences positives ou négatives? Je vais développer ce point précis en élaborant sur le jeûne comme un moyen de restriction calorique.
Le jeûne et la restriction calorique sont des habitudes de vie qui ont été récemment reconnues comme très pertinentes pour le maintien de la santé générale ou de la longévité. Ils sont considérés comme un « bon stress » physiologique parce qu’ils forcent le corps à s’adapter aux nouvelles conditions afin de retrouver l’équilibre. Par exemple, pour ce qui est de l’apport énergétique, ils forcent l’organisme à entrer en cétose (après 12-24 heures de jeûne); processus durant lequel le corps commencera à décomposer la graisse en réserve au lieu d’utiliser du glucose comme source d’énergie.
Considérant ces bénéfices, le jeûne excessif entraîne-t-il des résultats positifs ou négatifs sur l’autophagie? Est-ce que le jeûne à court terme ou le jeûne à long terme aiderait ou mettrait en danger les mécanismes de l’autophagie? Tel que mentionné dans l’article précédent, l’autophagie peut parfois être provoquée par des pathogènes et des cancers pour leurs propres bénéfices plutôt que le nôtre. Serait-ce dommageable ou utile? Voyons voir…
À court terme vs. À long terme
En adoptant le jeûne pour une période approximative de 6-8 heures, la macroautophagie s’enclenche. À ce stade du jeûne, afin que le corps s’approvisionne des sources nécessaires, la macroautophagie va détruire les composants cellulaires de façon aléatoire. Dépendamment de l’organe/des tissus, l’autophagie à plus long terme est activée après environ 12 heures de jeûne où l’autophagie provoquée par une protéine chaperon détruira les protéines non essentielles de façon sélective (voir le premier article pour la définition de ces deux types d’autophagie).
Le jeûne chronique/famine grave
Il a été démontré que le jeûne chronique inhibe la fonction de l’autophagie et peut donc conduire à des dommages neuronaux plutôt que de bénéficier à l’individu dans sa globalité. Dans certains cas, ceci peut résulter d’une famine sévère. Comme vous pouvez l’imaginer, dans des conditions chroniques sévères, les niveaux de stress et de balance énergétique dans le corps atteindraient un point où l’autophagie pourrait créer trop de dommage si elle devait être maintenue comme elle le ferait dans des conditions normales. Cela a du sens, car l’autophagie devrait, à ce point, détruire les protéines essentielles afin de soutenir la survie. C’est pourquoi, sous le jeûne chronique, l’autophagie serait en quelque sorte inhibée et ne serait initiée que comme moyen de survie. C’est seulement dans des cas sévères ou chroniques que les effets de « recyclage » de l’autophagie seraient excessifs et provoqueraient une réponse négative sur le corps. Il n’y a donc pas de problème pour des jeûnes intermittents ou modérés.
L’autophagie, le jeûne et la longévité
Depuis que la restriction calorique et les mimétiques de la restriction calorique sont liés à la longévité, la question suivante demeure : les bénéfices santé de la restriction calorique proviennent-ils de l’action de l’autophagie? Est-ce le contraire? Ou les voies de signalisation cellulaire et le métabolisme cellulaire sont-ils davantage impliqués dans les bénéfices santé?
Il y a un grand nombre de composantes impliquées dans la signalisation cellulaire de l’autophagie et de la restriction calorique. Ces voies de signalisation qui font partie du métabolisme de la cellule, et régule l’autophagie, sont principalement celles du mTOR et de l’AMPK.
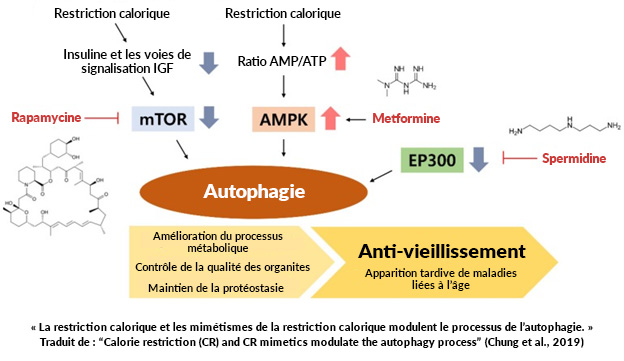
Les voies mTOR et AMPK
Chez les mammifères, la rapamycine (un mimétique de la restriction calorique; un agent gérosuppresseur) cible une molécule de signalisation (le mTOR) qui module la croissance/prolifération cellulaire, l’homéostasie énergique ainsi que l’autophagie. Elle est formée de complexes; le complexe mTOR 1 (TORC1) et le complexe mTOR 2 (TORC2) qui sont généralement régulés/régies par :
- Les facteurs de croissance,
- Les facteurs de stress cellulaire,
- Le niveau d’énergie.
L’autophagie est aussi régie/régulée par l’une des principales protéines de signalisation sensibles aux nutriments; la protéine kinase activée par l’AMP (AMPK). Ce que nous ne voyons pas sur l’image ci-haut, c’est lorsque l’AMPK est activé, il diminue automatiquement l’activation de la mTOR. Donc, sous les conditions de la restriction calorique/le jeûne, les niveaux d’insuline ainsi que les voies de signalisation de facteur de croissance de l’insuline (IGF) diminueront. Ceci diminuera l’action de la signalisation de la mTOR qui, à son tour, activera l’autophagie. Sous les mêmes conditions, les niveaux d’énergie baisseront (baisse des niveaux d’ATP; la principale source d’énergie du corps) et les niveaux d’AMP augmenteront.
** Lors de l’utilisation de l’énergie dans le corps, l’ATP, l’adénosine triphosphate (trois groupes de phosphate) subit une hydrolyse pour éventuellement se retrouver avec seulement un groupement phosphate, l’AMP (adénosine monophosphate). Pour mieux comprendre les processus par lesquelles le glucose est décomposé en énergie cellulaire (ATP) et utilisée comme énergie à travers le corps, je suggère de revoir la respiration cellulaire et toutes ses complexités. **
Lorsque les niveaux d’AMP augmentent, la cellule comprend qu’elle est entrain de manquer d’énergie; l’AMPK est activé, ce qui active l’autophagie et réduit l’action de la mTOR (afin de freiner le développement). Une fois que vous comprenez l’essentiel de ces voies de signalisation, tout ceci a du sens et fonctionne de manière semblable à des dominos, car lorsqu’une seule pièce tombe, toutes les autres tomberont par la suite (c’est ce que les scientifiques appellent une cascade de signalisation où le stimulus d’un élément crée une réaction en chaîne). Pour faire simple, les cellules ont la capacité d’évaluer l’état énergétique, le niveau d’énergie disponible, afin de savoir quand ralentir le développement et démarrer les processus de recyclage.
Ce qui est intéressant de noter par rapport à l’image ci-dessus, c’est qu’il y a des molécules qui peuvent induire ou inhiber ces voies qui ont des effets antivieillissement; les plus connues seraient la rapamycine, la metformine et la spermidine (qui sont aussi considérées comme des mimétiques de la restriction calorique ou des agents gérosuppresseurs). La voie du complexe mTOR 1 (TORC1) est celle à laquelle l’on se réfère habituellement lorsqu’il est question des voies de la longévité et de leur régulation. La raison pour laquelle je vous le mentionne, c’est que les processus de l’autophagie diminuent avec l’âge et cette réduction est corrélée avec l’augmentation de la fréquence des maladies associées au vieillissement. Ainsi, l’usage des mimétiques (gérosuppresseurs) et du jeûne pour leur effet sur la longévité pourrait possiblement être révolutionnaire!
L’autophagie, le jeûne et la réponse immunitaire
Le vieillissement en général est attribué à plusieurs facteurs. L’autophagie a un rôle évident sur le vieillissement, comme je l’ai mentionné précédemment. Ce sujet sera davantage exploré dans mon prochain article où je discuterai de l’effet des sirtuines et des produits naturels sur l’autophagie.
À ce point-ci, vous pouvez imaginer, avec toutes les informations fournies, l’impact de l’autophagie sur les maladies en générale et sur celles liées au vieillissement. Les bénéfices du jeûne, en ce qui concerne les maladies et l’implication du système immunitaire, proviennent de la réduction de l’inflammation (un avantage pour beaucoup de maladies) et de l’augmentation de la résistance cellulaire qui renforcera les capacités immunitaires. Je vais profiter de l’occasion pour utiliser la pandémie actuelle, la Covid-19, comme exemple. Tel que mentionné dans l’article précédent, l’autophagie est aussi impliquée, avec la présentation de l’antigène et la signalisation cellulaire, dans la réponse immunitaire. Dans le cas du jeûne et de l’autophagie, l’action du système immunitaire serait amplifiée. Selon Hannan et ses collaborateurs (2020), « la restriction calorique sous forme de jeûne intermittent, a permis dans plusieurs milieux cliniques de promouvoir de nombreux bénéfices santé incluant l’augmentation de l’efficacité du système immunitaire » (Traduction libre).
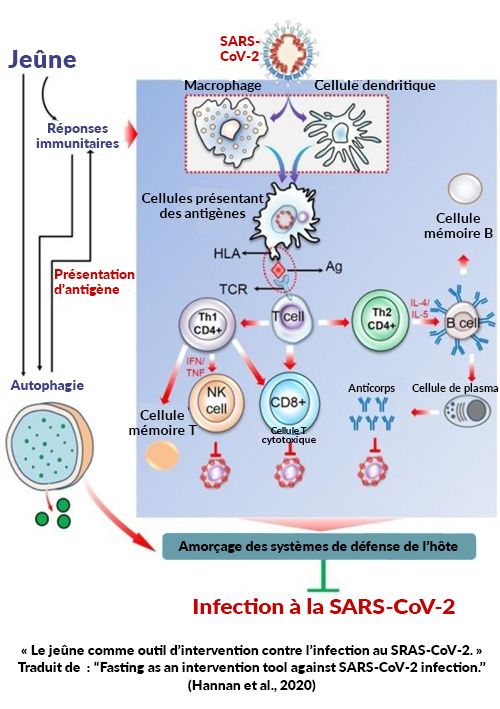
Même si la pandémie est trop récente pour fournir des résultats scientifiques concernant cette théorie/stratégie, les études actuelles fournissent des hypothèses positives. Malgré qu’il n’y ait pas de remède pour ce virus, les avantages du jeûne comme méthode de prévention quand le système immunitaire serait compromis, pourraient être utilisés comme un outil peu coûteux et potentiellement efficace. Notez cependant qu’il n’est pas recommandé de jeûner lors des périodes d’infection puisque le corps ne doit pas avoir de carence en nutriments ou un stress nutritionnel dans de telles conditions. Si vous choisissez de jeûner durant une période où votre système immunitaire est affaibli (comme ce serait le cas pour quelques maladies et les thérapies contre le cancer que j’aborde dans le paragraphe suivant), il serait recommandé d’être suivi par un professionnel de la santé. Le jeûne pris en exemple avec la Covid-19 est un moyen de stimuler le système immunitaire afin d’activer l’autophagie et les réponses immunitaires pour prévenir l’apparition de l’infection.
Dans le cas d’un cancer, le jeûne est apparu comme un moyen efficace d’améliorer l’action de l’autophagie tout en étant bénéfique lorsqu’il est combiné à d’autres thérapies de traitement. Dans l’article précédent, j’ai mentionné que l’autophagie élimine la formation de nouvelle tumeur et recyclera les organites ainsi que les protéines endommagées. Ainsi, la modulation de l’autophagie par le jeûne pourrait procurer des bénéfices anticancéreux. Ce domaine de recherche est assez complexe puisqu’il y a plusieurs facteurs qui interviennent concernant le type de cancer, la progression, les thérapies utilisées, etc. C’est la raison pour laquelle il est recommandé de consulter ou d’être suivi par un professionnel dans le cas où vous choisissez de jeûner tout en combattant un cancer ou toute autre maladie chronique.
Conclusion
Pour résumer, les processus de l’autophagie peuvent être modulés par le jeûne et/ou la restriction calorique. Il y a encore beaucoup de recherches à faire, mais on ne peut qu’imaginer les bienfaits thérapeutiques ainsi que leurs utilisations pour les conditions de défenses immunitaires telles que la Covid-19, les maladies liées au vieillissement ainsi que les cancers! Le potentiel de l’usage de l’autophagie et du jeûne serait presque infini s’il existait un moyen direct de bien le contrôler. Considérant le fait que le jeûne/la restriction calorique est une approche sécuritaire que tous peuvent intégrer facilement, à leur façon, dans leur vie quotidienne, les possibilités de bénéfices sont extrêmement excitantes; il va sans dire que la tendance de la diète cétogène a du sens!
La prochaine fois que vous jeûnerez, que ce soit pour des raisons religieuses, pour perdre du poids ou simplement parce que vous n’avez pas le temps de manger dû au fait que vous êtes trop occupé; pensez à quel point vos systèmes d’autophagie sont heureux en rétablissant l’homéostasie dans toutes vos cellules et vos tissus! Restez à l’affût pour le prochain article sur l’autophagie où j’approfondirai et discuterai de ses implications encore plus en détail concernant la longévité, les produits naturels et les sirtuines!
J’espère que vous avez apprécié cet article et je vais continuer mes recherches afin de vous offrir d’autres textes sur des sujets variés dans le domaine de la santé! Écrivez-nous un message pour toutes questions ou demande de renseignements.
Autres sujets proposés :
- Le jeûne, article 1 : Les bases biologiques de la réflexion
- Le jeûne article 4 : Stimuler la réparation et ralentir le vieillissement
- L’ultime médecine préventive; ça vous dit quelque chose?
Références:
- Bagherniya M, Butler AE, Barreto GE, Sahebkar A. The effect of fasting or calorie restriction on autophagy induction: A review of the literature. Ageing Res Rev. 2018;47:183-197. doi:10.1016/j.arr.2018.08.004
- Morselli E, Maiuri MC, Markaki M, et al. Caloric restriction and resveratrol promote longevity through the Sirtuin-1-dependent induction of autophagy. Cell Death Dis. 2010;1(1):e10. Doi:10.1038/cddis.2009.8
- Varghese N, Werner S, Grimm A, Eckert A. Dietary Mitophagy Enhancer: A Strategy for Healthy Brain Aging? Antioxidants (Basel). 2020 Sep 29;9(10):E932. doi: 10.3390/antiox9100932. PMID: 33003315.
- Alirezaei M, Kemball CC, Flynn CT, Wood MR, Whitton JL, Kiosses WB. Short-term fasting induces profound neuronal autophagy. Autophagy. 2010;6(6):702-710. doi:10.4161/auto.6.6.12376
- Antunes F, Erustes AG, Costa AJ, et al. Autophagy and intermittent fasting: the connection for cancer therapy?. Clinics (Sao Paulo). 2018;73(suppl 1):e814s. Published 2018 Dec 10. doi:10.6061/clinics/2018/e814s
- Cuervo, A., Wong, E. Chaperone-mediated autophagy: roles in disease and aging. Cell Res 24, 92–104 (2013). https://doi.org/10.1038/cr.2013.153
- Bejarano E, Cuervo AM. Chaperone-mediated autophagy. Proc Am Thorac Soc. 2010;7(1):29-39. doi:10.1513/pats.200909-102JS
- Glick D, Barth S, Macleod KF. Autophagy: cellular and molecular mechanisms. J Pathol. 2010;221(1):3-12. doi:10.1002/path.2697
- Parzych KR, Klionsky DJ. An overview of autophagy: morphology, mechanism, and regulation. Antioxid Redox Signal. 2014;20(3):460-473. doi:10.1089/ars.2013.5371
- Schuck, Sebastian. Microautophagy – distinct molecular mechanisms handle cargoes of many sizes. Journal of Cell Science. Published 9 September 2020; 133: jcs246322 doi: 10.1242/jcs.246322
- Ju Huang & Daniel J. Klionsky (2007) Autophagy and Human Disease, Cell Cycle, 6:15, 1837-1849, DOI: 10.4161/cc.6.15.4511
- Nakamura S, Yoshimori T. Autophagy and Longevity. Mol Cells. 2018;41(1):65-72. doi:10.14348/molcells.2018.2333
- Hannan MA, Rahman MA, Rahman MS, et al. Intermittent fasting, a possible priming tool for host defense against SARS-CoV-2 infection: Crosstalk among calorie restriction, autophagy and immune response. Immunol Lett. 2020;226:38-45. doi:10.1016/j.imlet.2020.07.001
- Chung KW, Chung HY. The Effects of Calorie Restriction on Autophagy: Role on Aging Intervention. Nutrients. 2019;11(12):2923. Published 2019 Dec 2. doi:10.3390/nu11122923
- Blagosklonny MV. From causes of aging to death from COVID-19. Aging (Albany NY). 2020 Jun 12;12(11):10004-10021. doi: 10.18632/aging.103493. Epub 2020 Jun 12. PMID: 32534452; PMCID: PMC7346074.






C’est très intéressant. Merci !
Merci à vous !