Sommaire
Le corps est un système complexe qui est tout à fait remarquable. Comme je l’ai déjà mentionné dans l’article Le concept de l’antivieillissement comme prévention contre la COVID-19?, le corps a différentes formes de programmes de maintenance pour s’assurer que toutes les parties soient fonctionnelles. C’est tout de même philosophique de penser à notre corps comme étant un système automatisé complexe, car nous vivons notre vie quotidienne sans avoir la moindre idée de ce qui se passe réellement, sur une microéchelle ou même macro, lors d’un battement de cœur!
C’est votre programme de maintenance qui entre en jeu lorsqu’il est question de conserver le bon fonctionnement d’un système aussi complexe à des conditions optimales alors que des dysfonctionnements surviennent. Je vais en profiter pour approfondir le monde de l’autophagie et son rôle sur notre système biologique ainsi que son rôle en lien avec les maladies et la longévité. Puisqu’il y a beaucoup de choses à dire sur le sujet, je vais séparer le tout en plusieurs segments. Je sais que ces thèmes peuvent devenir un peu lourds, précisément si plusieurs termes sont nouveaux. Une pause-café pourrait être bien méritée au cours de cette lecture! Dans mes prochains articles, je vais explorer l’implication des produits naturels et des saines habitudes de vie en ce qui concerne l’autophagie.
Un système de recyclage biologique
L’autophagie est un système de « nettoyage » (un « rôle d’entretien ») qui va arriver d’un coup et s’appliquer lorsque quelque chose fonctionne mal ou est influencé par le stress, avant qu’un dommage majeur ne survienne. L’autophagie est vraiment importante en santé humaine, car ses mécanismes de recyclage peuvent rendre des cellules fonctionnelles à nouveau en permettant la réparation de certaines fonctions ou encore, en retirant les déchets qui interfèrent avec le bon fonctionnement des cellules comme c’est le cas avec la maladie d’Alzheimer. C’est un processus crucial qui se produit dans certaines circonstances telles que :
- Les étapes de développement,
- En réponse à un stress nutritionnel,
- Lorsqu’il y a un dysfonctionnement ou lors de l’agrégation de protéines,
- Pour éliminer les organites endommagés (mitochondries, réticulum endoplasmique et peroxysomes),
- Pour éliminer les pathogènes intracellulaires,
- Pour réagir à des situations extrêmes comme un faible niveau d’oxygène.
L’efficacité avant tout
Votre corps souhaite être le plus efficace possible et lorsqu’il est question de ses ressources, il veut obtenir le meilleur de chaque situation donnée. Pour survivre, c’est essentiel! Il est important de souligner ici, que ces processus d’autophagie entrent en jeu, pas uniquement lors des situations énumérées auparavant, mais dans toutes les tâches reliées au dysfonctionnement ou au stress biologique. Ils agiront donc pour :
- Permettre la sénescence cellulaire,
- Activer la présentation des antigènes de surface cellulaire (qui est une forme de communication cellulaire (c’est-à-dire la signalisation cellulaire) pour que le corps comprenne ce qu’il doit faire par la suite, comme déclencher une réponse immunitaire, etc.),
- Protéger contre l’instabilité du génome,
- Prévenir la nécrose (mort prématurée de cellules vivantes et de tissus corporels),
- Mobiliser les réserves d’énergie,
- Supprimer la formation tumorale,
- Recycler les organites endommagés dans les conditions suivantes : Les stress du réticulum endoplasmique, l’hypoxie (carence d’oxygène dans les tissus), un manque de nutriments, une accumulation de protéines anormales ou des dommages à l’ADN.
Quand la vie vous donne des citrons, l’autophagie sait définitivement comment faire de la limonade! Puisqu’elle a un rôle essentiel chez l’homme (et les organismes en général), celle-ci est aussi régulée et catégorisée en trois types; qui favorisent la dégradation des composants cytosoliques (à l’intérieur de la cellule) défectueux/envahissants via le lysosome (un genre de ‘’blob’’ digestif). Ces trois types sont :
- Microautophagie,
- Macroautophagie et
- Autophagie provoquée par une protéine chaperon.
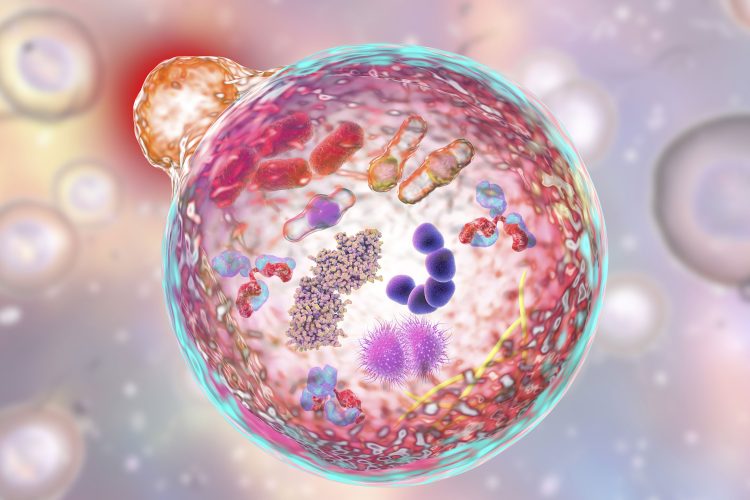
1. Microautophagie :
Tel que démontré sur l’image ci-haut à droite, par Bajarano et ses collaborateurs, la microautophagie est le processus de dégradation à microéchelle (les petits morceaux qui doivent être recyclés). Ces composantes sont dirigées vers le lysosome et sont directement prises dans le lysosome par une forme d’invagination de la membrane lysosomale. Le mécanisme exact derrière la microautophagie est toujours étudié par les chercheurs, mais elle est considérée comme étant le principal type d’autophagie responsable du renouvellement des organites et des protéines dans toutes les cellules. Chez les humains, lorsqu’il y a une carence en acides aminés, les protéines cytosoliques sont détruites par ce type d’autophagie pour récupérer les acides aminés essentiels. Il a la capacité de travailler avec des mécanismes sélectifs et non sélectifs qui implique que certains de ces processus requièrent une signalisation spécifique et des étapes prédéfinies, alors que certains ne le font pas.
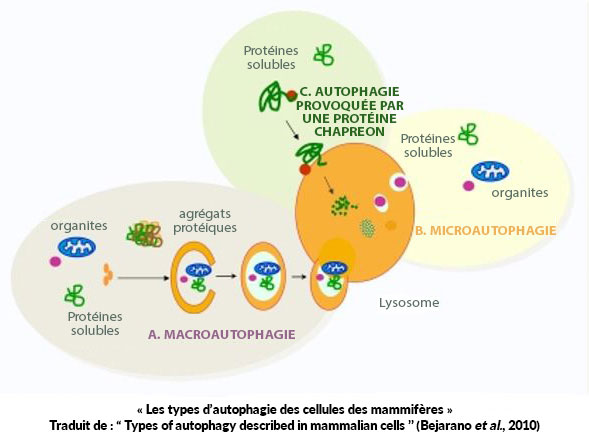
2. Macroautophagie :
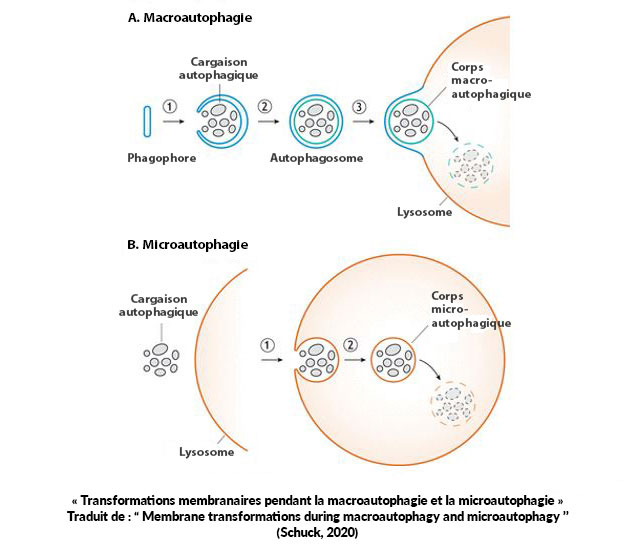
La macroautophagie est l’un des types d’autophagie le plus étudié et il est lié à plusieurs maladies chez l’humain (j’y reviendrai plus tard dans cet article ainsi que dans mon prochain article). Ce type de recyclage considère habituellement des composantes comme des organites endommagés ou des protéines mal repliées, comme la microautophagie, mais il incorpore l’agrégation des protéines dans son mécanisme de transport (qui est très différent) pour effectuer de grandes dégradations. Comme la micoautophagie, elle fonctionne aussi avec des mécanismes sélectifs et non sélectifs. La macroautophagie crée un phagophore qui, une fois complété, est appelé l’autophagosome, qui entoure le composant à recycler (ce que les scientifiques appellent une cargaison cytoplasmique/autophagique) qui sera envoyé au lysosome pour élimination. Nous pourrions faire un parallèle avec les camions qui récupèrent nos matériaux recyclables. Ce sont des véhicules de transport qui prennent les matériaux endommagés de l’appareil de récupération (les lysosomes). Cet autophagosome est une vésicule à double membrane qui fusionne avec la membrane du lysosome afin d’expulser ces composantes pour les éliminer (comme illustré dans l’image ci-dessous).
3. Autophagie provoquée par une protéine chaperon :
L’autophagie provoquée par une protéine chaperon fonctionne très différemment des deux autres types. Les protéines chaperon servent à réactiver des protéines mal repliées. On pourrait définir le chaperon un peu comme une personne qui aurait pour objectif de surveiller/superviser quelque chose. S’il ne réussit pas à rendre la protéine à nouveau fonctionnelle, il y restera attaché pour former un complexe d’identification et il engendrera sa récupération pour être recyclée.
Un complexe chaperon est nécessaire afin d’identifier les protéines solubles à apporter au lysosome pour la destruction. Celles-ci travaillent seulement avec des mécanismes sélectifs qui sont beaucoup plus complexes puisque les protéines chaperons (comme les protéines à choc thermique) sont reconnues par un récepteur lysosomique (protéine membranaire lysosomique), qui travaillent ensemble, dans plusieurs cas, pour le recyclage. C’est comme si un employé d’un concessionnaire automobile usagé avait identifié celles qui pouvaient être détruites afin de réutiliser les pièces de métal et qu’il avait alors donné le signal « de les détruire ».
L’autophagie provoquée par une protéine chaperon est seulement dédiée à la dégradation des protéines solubles pas le processus sélectif de reconnaissance des acides aminés de la protéine. C’est un long processus qui comprend beaucoup d’exigences pour que la cargaison entre complètement dans le lysosome. Ce qui rend l’autophagie provoquée par une protéine chaperon si intéressante, c’est que son processus est si spécifique qu’il peut identifier des protéines précises sans perturber les autres protéines environnantes de manière efficace et effective. Pour continuer avec le même exemple, ce type d’autophagie est capable de sélectionner les voitures qui ne fonctionnent plus. Les exigences énergétiques, de signalement et de stress ainsi que beaucoup de détails spécifiques en lien avec le processus de l’autophagie provoquée par une protéine chaperon sont encore étudiées à ce jour.
L’autophagie et la longévité
Nous savons déjà que les processus de l’autophagie sont plus efficaces dans les organismes ayant une plus longue longévité. Tout au long de la vie, les processus de l’autophagie ont tendance à diminuer. D’autres facteurs, tels qu’une mauvaise alimentation, peuvent avoir tendance à diminuer leurs fonctions, ce qui à son tour, pourrait favoriser l’apparition de plusieurs maladies. Vous pouvez voir ici que c’est très similaire au concept de la poule et de l’œuf où la diminution de la fonction de l’autophagie peut conduire à la maladie alors que la fonction de l’autophagie tend à diminuer avec l’âge, ce qui provoque l’apparition des maladies liées au vieillissement. Je vais élaborer davantage sur le lien entre l’autophagie et la longévité dans le prochain article. Je vous recommande donc de rester à l’affût des nouveaux articles sur le blogue de Vitoli.
L’autophagie et les maladies
L’autophagie joue un rôle majeur pour notre santé, en passant par la suppression d’une tumeur jusqu’à promouvoir la survie cellulaire, la mort cellulaire et le recyclage cellulaire. En fait, l’autophagie est un système d’adaptation cellulaire face aux conditions difficiles (ce que l’on appelle un stress cellulaire). Toutes les situations qui changent les conditions homéostatiques où le corps doit s’adapter pour retrouver l’équilibre. Dans mon prochain article, je vais parler d’un stress bénéfique; le jeûne.
Comme mentionné par Glick et ses collaborateurs, « En plus de l’élimination des agrégats intracellulaires et des organites endommagés, l’autophagie favorise la sénescence cellulaire et la présentation des antigènes de surface des cellules, protège contre l’instabilité du génome et prévient la nécrose, ce qui lui donne un rôle clé dans la prévention des maladies telles que le cancer, la neurodégénérescence, la cardiomyopathie, le diabète, les maladies du foie, les maladies auto-immunes et les infections (Traduction libre). »
Certaines des multiples maladies associées au mécanisme et/ou dysfonctions de l’autophagie incluent :
- La maladie de Parkinson,
- La maladie de Huntington,
- La sclérose latérale amyotrophique (SLA),
- La maladie d’Alzheimer,
- La dégénérescence fronto-temporale (DFT),
- La maladie de Danon,
- La maladie de Crohn,
- Le cancer du sein, des ovaires, du colon et de la prostate,
- La maladie de Batten,
- La maladie de Paget
- Etc.
« Cependant, l’importance des défauts de l’autophagie pour la maladie et le vieillissement est évidente à partir de preuves grandissantes reliant la mutation ou la perte de fonction des gènes de l’autophagie dans le cancer, les neuropathies, les maladies du cœur, les maladies auto-immunes et d’autres conditions. Du point de vue d’un biologiste du cancer, le fait que l’autophagie supprime les tumeurs (par arrêt du cycle cellulaire, par la promotion de l’intégrité du génome et des organites ou par inhibition de la nécrose et de l’inflammation) ou oncogènes (en favorisant la survie des cellules face au stress nutritionnel spontané ou induit) reste un sujet controversé. Pour d’autres maladies comme les neuropathies (maladie de Huntington, l’Alzheimer et le Parkinson) et les maladies cardiaques ischémiques, l’autophagie est plus largement acceptée comme bénéfique dû à son rôle dans l’élimination des actifs toxiques et de la promotion de la viabilité des cellules. Donc, l’autophagie est apparue comme un nouveau et puissant modulateur de la progression des maladies qui est à la fois intrigant et cliniquement pertinent. »
(Glick et al., 2010) (Traduction libre)
Malgré le fait que l’autophagie a une grande capacité à maintenir la santé et la longévité, elle a aussi ses implications négatives dans la santé. Certains pathogènes (bactéries et virus) peuvent parfois manipuler ces mécanismes étonnants à leur avantage. De même, parfois les cancers utilisent les mécanismes cytoprotecteurs qui leurs permettent de résister à de nombreux traitements. C’est pourquoi les mécanismes complets ainsi que leurs déclencheurs/signaux sont toujours étudiés par les chercheurs. Il y a beaucoup de potentiel au fait que ces systèmes soient utilisés pour des traitements qui permettraient de désactiver la manipulation pathogène/cancer de ces mécanismes et de détecter leur apparition afin d’éviter ces maladies.
J’espère que vous avez apprécié cet article! Je vais continuer de m’informer pour vous écrire sur d’autres sujets pertinents dans le domaine de la santé! N’hésitez pas à nous envoyer un message pour toutes questions ou commentaires. info@vitoli.com
Autres textes à consulter :
- Le jeûne, article 1 : les bases biologiques de la réflexion
- Produits naturels et sirtuines; Comment prévenir les maladies?
- Le concept de l’antivieillissement comme prévention contre la Covid-19?
- Système immunitaire 2 de 2 : 6 suppléments efficaces
Références:
- Bagherniya M, Butler AE, Barreto GE, Sahebkar A. The effect of fasting or calorie restriction on autophagy induction: A review of the literature. Ageing Res Rev. 2018;47:183-197. doi:10.1016/j.arr.2018.08.004
- Morselli E, Maiuri MC, Markaki M, et al. Caloric restriction and resveratrol promote longevity through the Sirtuin-1-dependent induction of autophagy. Cell Death Dis. 2010;1(1):e10. Doi:10.1038/cddis.2009.8
- Varghese N, Werner S, Grimm A, Eckert A. Dietary Mitophagy Enhancer: A Strategy for Healthy Brain Aging? Antioxidants (Basel). 2020 Sep 29;9(10):E932. doi: 10.3390/antiox9100932. PMID: 33003315.
- Alirezaei M, Kemball CC, Flynn CT, Wood MR, Whitton JL, Kiosses WB. Short-term fasting induces profound neuronal autophagy. Autophagy. 2010;6(6):702-710. doi:10.4161/auto.6.6.12376
- Antunes F, Erustes AG, Costa AJ, et al. Autophagy and intermittent fasting: the connection for cancer therapy?. Clinics (Sao Paulo). 2018;73(suppl 1):e814s. Published 2018 Dec 10. doi:10.6061/clinics/2018/e814s
- Cuervo, A., Wong, E. Chaperone-mediated autophagy: roles in disease and aging. Cell Res 24, 92–104 (2013). https://doi.org/10.1038/cr.2013.153
- Bejarano E, Cuervo AM. Chaperone-mediated autophagy. Proc Am Thorac Soc. 2010;7(1):29-39. doi:10.1513/pats.200909-102JS
- Glick D, Barth S, Macleod KF. Autophagy: cellular and molecular mechanisms. J Pathol. 2010;221(1):3-12. doi:10.1002/path.2697
- Parzych KR, Klionsky DJ. An overview of autophagy: morphology, mechanism, and regulation. Antioxid Redox Signal. 2014;20(3):460-473. doi:10.1089/ars.2013.5371
- Schuck, Sebastian. Microautophagy – distinct molecular mechanisms handle cargoes of many sizes. Journal of Cell Science. Published 9 September 2020; 133: jcs246322 doi: 10.1242/jcs.246322
- Ju Huang & Daniel J. Klionsky (2007) Autophagy and Human Disease, Cell Cycle, 6:15, 1837-1849, DOI: 10.4161/cc.6.15.4511
- Nakamura S, Yoshimori T. Autophagy and Longevity. Mol Cells. 2018;41(1):65-72. doi:10.14348/molcells.2018.2333